علماء ألمانيا يبتكرون 'رقعة الحياة' لإصلاح القلوب التالفة
غوتينغن (ألمانيا) - في اختراق طبي وُصف بأنه "المقدس" في طب القلب التجديدي، كشفت تقارير طبية صادرة في الأسبوع الأخير من عام 2025 عن نجاح تجارب سريرية لاستخدام أنسجة قلبية مهندسة وراثياً لترميم قلوب مرضى يعانون من فشل قلبي حاد، محققة نتائج غير مسبوقة باستعادة 40 بالمئة من الوظائف الحركية المفقودة للعضلة القلبية.
هذا التطور، الذي يأتي ضمن حصاد العام الطبي لعام 2025، يضع حدا لعقود من المحاولات الفاشلة لإصلاح الأضرار الدائمة التي تسببها السكتات القلبية، ويفتح الباب أمام بديل حيوي حقيقي لعمليات زراعة القلب التقليدية التي تعاني من نقص حاد في المتبرعين.
"عضلة من المختبر"
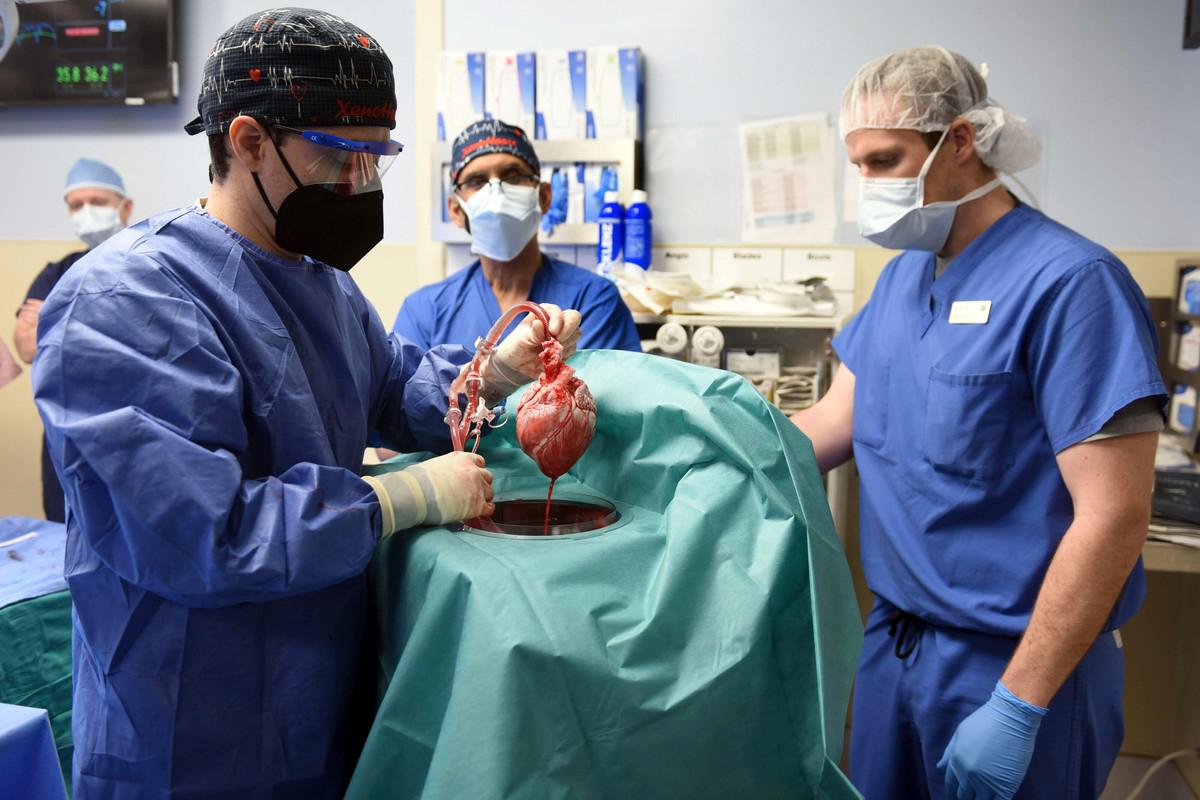
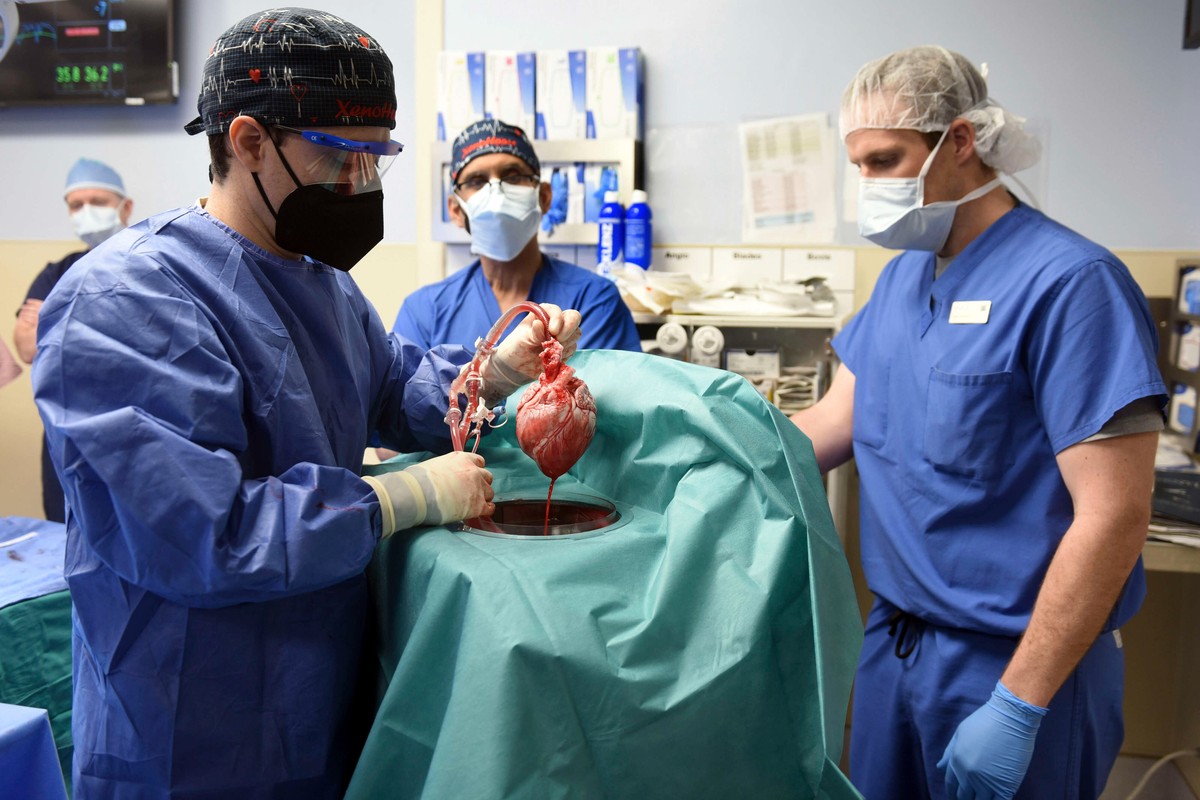
بدأت القصة في المركز الطبي لجامعة غوتينغن بألمانيا (UMG)، حيث قاد البروفيسور فولفرام-هوبرتوس زيمرمان فريقاً بحثياً لتطوير ما يُعرف بـ "نسيج القلب البشري المهندس" (EHM). وتعتمد التقنية على تحويل الخلايا الجذعية المستحثة (iPSCs) المأخوذة من المريض نفسه أو من متبرعين عالميين إلى خلايا عضلية قلبية نابضة.
ووفقاً للبيانات التي اطلعت عليها "رويترز" من تجربة "BioVAT-HF"، لم يتم حقن هذه الخلايا بشكل عشوائي كما كان متبعاً في السابق، بل جرى استنباتها داخل قالب من الكولاجين لتشكيل "رقعة قلبية" حية (Heart Patch). ويكمن السر في النجاح المحقق هذا العام في استخدام الهندسة الوراثية لتعزيز قدرة هذه الرقعة على "التوعية الدموية" السريعة، مما سمح لها بالاندماج مع الدورة الدموية للمريض في غضون أيام قليلة من الجراحة.
لغة الأرقام: قفزة في الأداء
ويقول محللون طبيون إن رقم "40 بالمئة" الذي سجله التقرير يمثل تحولاً جذرياً؛ ففي حالات فشل القلب الانتهائي، تتراجع قدرة القلب على ضخ الدم (الكسر القذفي) إلى مستويات حرجة تهدد الحياة. واستعادة اكثر من ثلث الوظائف التي فُقدت نتيجة التليف يعني عملياً نقل المريض من حالة العجز الكامل والاعتماد على أجهزة المساعدة الميكانيكية إلى حالة الاستقرار السريري والقدرة على ممارسة النشاط البدني المعتدل.
نحن لا نضع ضمادة على الجرح، بل نضيف محركاً جديداً للقلب
وصرح البروفيسور زيمرمان في تعليق تقني: "نحن لا نضع ضمادة على الجرح، بل نضيف محركاً جديداً للقلب. الرقعة التي تحتوي على ما يصل إلى 800 مليون خلية حية لم تدعم القلب ميكانيكياً فحسب، بل اندمجت معه كهربائياً، مما يعني أنها تنبض بتناغم تام مع نبضات القلب الأصلية".
الجراحة والاستجابة السريرية
شملت المرحلة الأخيرة من التجارب في عام 2025 مجموعة من المرضى الذين كان الخيار الوحيد المتبقي أمامهم هو زراعة قلب كامل. وأجريت العمليات باستخدام تقنيات جراحية محدودة التدخل، حيث تم تثبيت الرقع المهندسة مباشرة على المناطق المتليفة من البطين الأيسر.
وأظهرت الفحوصات بالأشعة المقطعية المتقدمة (CT) والرنين المغناطيسي القلبي (MRI) أن الأنسجة المزروعة بدأت في النمو والسمك بمرور الوقت، محاكيةً سلوك العضلة القلبية الطبيعية. والأهم من ذلك، لم تُسجل حالات رفض مناعي كبرى بفضل التعديلات الوراثية التي جعلت الأنسجة "غير مرئية" تقريباً لجهاز المناعة.
التأثير الاقتصادي واللوجستي
من المتوقع أن يغير هذا الاختراق خريطة الإنفاق الصحي العالمي. فتكلفة زراعة القلب وصيانتها بالأدوية المثبطة للمناعة مدى الحياة تفوق بكثير تكلفة إنتاج هذه الرقع الحيوية. ويشير تقرير حصاد العام إلى أن التوجه في 2026 سينصب نحو إنتاج هذه الرقع "على الرف" (Off-the-shelf)، بحيث يمكن للمستشفيات طلبها واستخدامها فوراً للمرضى الذين يعانون من احتشاء عضلة القلب الحاد لمنع تحوله إلى فشل دائم.
ومع اقتراب عام 2026، تتجه الأنظار نحو الهيئات التنظيمية مثل إدارة الغذاء والدواء الأميركية (FDA) ووكالة الأدوية الأوروبية (EMA) للحصول على الاعتمادات النهائية للمرحلة الثالثة، وسط توقعات بأن تصبح هذه التقنية معياراً علاجياً جديداً بحلول عام 2027.
وقال الدكتور جيمس برادلي، استشاري جراحة القلب في لندن: "إذا استمرت هذه النتائج في الثبات، فإننا نشهد نهاية عصر كان فيه تلف القلب حكماً بالإعدام البطيء. لقد انتقلنا من مرحلة الطب الترميمي النظري إلى التطبيق العملي الذي يعيد بناء الحياة".